(এই লেখাটার মূল উদ্দেশ্য হল আদর্শ গ্যাসের বেলায় যেকোনো প্রক্রিয়ায় এন্ট্রপির মান নির্ণয়ের জন্য একটি সাধারণ সমীকরণ তৈরি করে দেখানো এবং সেটা ব্যবহার করে বোল্টজম্যান-এন্ট্রপি সূত্রে থাকা ধ্রুবকের মান নির্ণয় করা। একইসাথে কোন প্রক্রিয়ার সাম্যাবস্থা ও সম্ভাব্যতার মাঝে কী ধরণের সম্পর্ক থাকে সেটার উপর আলোকপাত করা।)
মূল আলোচনায় যাবার আগে এই লেখার সাথে সম্পর্কিত যেসব ব্যাপার জানতে হবে সেগুলো বলে রাখি। সেগুলো হল এন্ট্রপি, গ্যাসের আয়তন বৃদ্ধিজনিত কাজ, সম্ভাব্যতা এবং বোল্টজম্যান-এন্ট্রপি সূত্রের প্রমাণ। এ বিষয়গুলো যতটা পারা যায় সহজে নিচের দুটি লেখায় বলা হয়েছে। –
১) এন্ট্রপি, সম্ভাব্যতা এবং বোল্টজম্যানের এন্ট্রপি-সূত্র
২) স্টিফেনের বিকিরণ সূত্রের প্রমাণঃ বিকিরণ ও তাপগতিবিদ্যা
এক্ষেত্রে কেউ চাইলে দু’টি নোটেরই প্রথম দিকের অংশটুকু পড়ে এসে অনায়াসে এই নোট পড়া শুরু করে দিতে পারে।
(তারপরও আগের নোটগুলোর কিছু কিছু অংশ তুলে ধরে লেখাটা শুরু করা হল।)
তাপগতিবিদ্যার প্রথম সূত্র বলে যে কোন বস্তুকে যদি তাপ দেয়া হয় তাহলে সেই তাপ দু’টি অংশে ভাগ হয়ে যেতে পারে। তাপের কিছু অংশ ব্যবহার করে বস্তুটি কাজ করতে পারে- বাকি অংশটুকু বস্তুর মাঝে অন্তর্নিহিত শক্তি হিসেবে জমা থাকে। বস্তুটিকে যদি কোন কাজ করতে দেয়া না হয় তাহলে তাপের পুরো অংশটুকুই তখন তার ভেতরে গিয়ে জমা হয়-অর্থাৎ বস্তুর অন্তর্নিহিত শক্তি বেড়ে যায়। কিন্তু তাই বলে আবার উল্টাটা হয় না- অর্থাৎ পুরো তাপকে বস্তু কাজে পরিণত করতে পারে না (তাপগতিবিদ্যার দ্বিতীয় সূত্র)। সুতরাং যদি বস্তুটি তাপ ব্যবহার করে তার কিছু অংশ কাজে পরিণত করে তাহলে অবশ্যই সাথে সাথে তার ভেতরকার অন্তর্নিহিত শক্তিও বেড়ে যাবে। যদি ΔQ পরিমাণ তাপ দেয়ার ফলে বস্তুটি ΔW পরিমাণ কাজ করে এবং তার অন্তর্নিহিত শক্তি ΔU পরিমাণ বেড়ে যায় তাহলে তাপগতিবিদ্যার প্রথম সূত্র মতে
ΔQ = ΔU + ΔW
আমাদের আলোচনার মূল বিষয় যেহেতু গ্যাসের সাথে জড়িত তাই আমরা বলতে পারি গ্যাস এই আলোচ্য ΔW পরিমাণ কাজ করে তার আয়তন বৃদ্ধির মাধ্যমে। যদি খুবই সামান্য পরিমাণ তাপ গ্যাসের মাঝে দেয়া হয় এবং তার আয়তন সামান্যই বাড়ে তাহলে এই আয়তন বৃদ্ধিকে ধরে নেয়া হয় যে সেটি আসলে স্থির চাপে হয়েছে। এই ধরে নেয়াটা তত সময় পর্যন্ত ঠিক থাকবে যত সময় পর্যন্ত তাপের পরিমাণ এবং আয়তন বৃদ্ধির মান খুবই ছোট হবে। এই ক্ষুদ্রাতিক্ষুদ্র পরিবর্তন দেখানোর জন্য আমরা পরবর্তিতে Δ চিহ্নের বদলে ‘d’ ব্যবহার করব। এখন স্থির চাপ ‘P’ তে যদি কোন গ্যাসের আয়তন ΔV বাড়ে তাহলে খুব সহজেই দেখানো যায় যে সেটি আয়তন বৃদ্ধিজনিত PΔV পরিমাণ কাজ করে।
সুতরাং ΔW = PΔV , ফলে
ΔQ = ΔU + PΔV ——————–(1)
এই সম্পর্কটি ঠিক দু’টি অবস্থায় সঠিক হবে। এক, যদি সব ধরণের পরিবর্তনের মান খুবই ছোট হয়- কারণ তখন চাপকে মোটামুটি স্থির ধরা যায় , এবং, দুই, যদি আগে থেকেই আয়তন বৃদ্ধির পুরো প্রক্রিয়াটি স্থির চাপে হবার ব্যবস্থা থাকে। এই ব্যাপারটা মাথায় রাখা খুবই গুরুত্বপূর্ণ, কেননা এমন প্রক্রিয়াও আছে যেখানে তাপ দিলে আয়তন বৃদ্ধির সাথে সাথে চাপও বেড়ে যায়। তাই কোনো কিছু উল্লেখ করা না থাকলে আমরা লিখি —
dQ = dU + dW এবং dW = P dV
সুতরাং, dQ = dU + P dV ———–(2)
এখানে এসে আমরা গ্যাসের সাথে সম্পর্কিত দু’টি রাশির ব্যাপারে আলোচনা করব।
দু’টি রাশির প্রতিটিই হল গ্যাসের মোলার-আপেক্ষিক-তাপ। আগে আসি আপেক্ষিক তাপের বিষয়ে। কোনো বস্তুর তাপমাত্রা একক পরিমাণ বাড়াতে বস্তুর প্রতি একক ভরের জন্য যে পরিমাণ তাপ সরবরাহ করতে হয় তাকে ঐ বস্তুর আপেক্ষিক তাপ বলে। লক্ষ্যনীয় যে এখানে তাপমাত্রার একক কী হবে (যেমন কেলভিন/ ডিগ্রী সেলসিয়াস/ ফারেনহাইট ইত্যাদি) কিংবা ভরের একক কী হবে (যেমন গ্রাম/কেজি/পাউণ্ড ইত্যাদি) সে ব্যাপারে কিছু বলা হয়নি। তাই ভিন্ন ভিন্ন একক ব্যবহার করলে কোনো বস্তুর আপেক্ষিক তাপের মান ভিন্ন ভিন্ন হয়। এবার আসি গ্যাসের মোলার-আপেক্ষিক-তাপের বিষয়ে। নাম থেকেই দেখা যাচ্ছে গ্যাসের পরিমাণ কত হবে সেটা আগেই বলে দেয়া আছে- অর্থাৎ গ্যাসের পরিমাণ হবে এক মোল। সুতরাং, এক মোল পরিমাণ গ্যাসের তাপমাত্রা এক একক (কেলভিন/ডিগ্রী সেলসিয়াস) বাড়াতে গ্যাসকে যে পরিমাণ তাপ দিতে হবে সেটাই হল গ্যাসের মোলার-আপেক্ষিক-তাপ। আয়তন স্থির রেখে গ্যাসকে তাপ দিলে তখন মোলার-আপেক্ষিক-তাপের যে মান পাওয়া যায় তাকে বলে স্থির আয়তনে গ্যাসের মোলার–আপেক্ষিক-তাপ। একে Cv দিয়ে প্রকাশ করা হয়।(C এর পাশে v দিয়ে বোঝাচ্ছে যে আয়তন স্থির রেখে গ্যাসের মোলার–আপেক্ষিক-তাপের মান বের করা হয়েছে।)
গ্যাসের বেলায় তাপমাত্রা বাড়ার সাথে সাথে আয়তন এবং চাপ দুটোই একসাথে বেড়ে যেতে পারে, অথবা শুধুই আয়তন বাড়তে পারে কিংবা শুধুই চাপ বাড়তে পারে। একসাথে বাড়ার বিষয়টাকে সহজ করার জন্য আমরা একে দু’টি আলাদা আলাদা অংশে ভাগ করে নিয়ে চিন্তা করি। ধরা যাক, প্রথমে আমরা গ্যাসকে আয়তনে বাড়তে না দিয়ে ঠিক যে তাপমাত্রায় সেটাকে শেষ পর্যন্ত আনতে হবে (T) সে তাপমাত্রায় পৌঁছানো পর্যন্ত তাপ দিলাম। আয়তনে বাড়তে না দেয়ার ফলে সেটার চাপ (P) বেড়ে যাবে। আদর্শ গ্যাসের বেলায় এই চাপ শেষ পর্যন্ত কত হবে সেটা আমরা চার্লসের সূত্র থেকে সহজেই বের করতে পারি(চাপ সমানুপাতিক পরম তাপমাত্রা)। নির্দিষ্ট তাপমাত্রায় পৌঁছানোর পরে আমরা গ্যাসকে প্রসারিত হতে দিব-তবে এবার সেটার চাপকে বাড়তে দিব না, এমনকি তাপমাত্রাও বাড়তে দিব না-কেবল তাপ সরবরাহ করে যাব (তাপের এই অংশটুকু কেবলমাত্র গ্যাসের আয়তন বৃদ্ধিতে খরচ হবে- অর্থাৎ এই তাপ গ্যাস তার আয়তন বৃদ্ধিতে পুরোপুরি কাজে লাগাবে। যদিও তাপগতিবিদ্যার দ্বিতীয় সূত্র মতে পুরো তাপ কখনোই কাজে পরিণত করা যায় না, তারপরও এটা ধরা সম্ভব হয়েছে পুরো ব্যাপারটাকে দু’টি আলাদা আলাদা অংশে আমরা চিন্তা করেছি বলে।) আয়তন বেড়ে আমাদের দরকারি আয়তনে (V) পৌছানোর পর আমরা তাপ দেয়া বন্ধ করে দিব। আমাদের মূল উদ্দেশ্য হল গ্যাসকে শেষ পর্যন্ত T তাপমাত্রায় P চাপে V আয়তনে আনা। প্রথম ধাপে যদি ΔQv পরিমাণ তাপ সরবরাহ করা হয় এবং দ্বিতীয় ধাপে যদি ΔQw পরিমাণ তাপ সরবরাহ করা হয় তাহলে মোট সববরাহকৃত তাপের পরিমাণ
ΔQ = ΔQv + ΔQw
যেহেতু প্রথম ধাপে স্থির আয়তনে তাপ দেয়া হয়েছে তাই স্থির আয়তনে গ্যাসের মোলার-আপেক্ষিক-তাপের (Cv) সংজ্ঞা ব্যবহার করে দেখানো যায় —
ΔQv = n Cv ΔT
এবং আয়তন বৃদ্ধিজনিত কাজ PΔV = ΔQw
সুতরাং, ΔQ = n Cv ΔT + PΔV ——–(3)
আবার, তাপগতিবিদ্যার প্রথম সূত্র মতে, (1) নং থেকে পাই
ΔQ = ΔU + PΔV
(3) নং এর সাথে মিলালে, ΔU + PΔV = n Cv ΔT + PΔV
বা, ΔU = n Cv ΔT (=ΔQv ) ————(4)
সুতরাং, (4) থেকে বলা যায় যে গ্যাসের বেলায় স্থির আয়তনে যতটুকু শক্তি দেয়া হয় তার পুরোটাই তার অন্তর্নিহিত শক্তির বৃদ্ধি ঘটায়। সাথে সাথে এটাও বলা যায় যে যদি তাপমাত্রার পরিবর্তন না হয় (সমোষ্ণ প্রক্রিয়ায়, ΔT=0) তাহলে গ্যাসের অন্তর্নিহিত শক্তির কোনো পরিবর্তন হয় না (ΔU=0)।
তাপের পরিমাণ, তাপমাত্রার বৃদ্ধি এবং আয়তন বৃদ্ধির মান খুবই ছোট হলে আমরা (3) নং এর জায়গায় লিখি
dQ = n Cv dT + P dV
এখন যদি তার এন্ট্রপির পরিবর্তন dS হয় তাহলে
dS = dQ/T , বা, dQ = TdS
সুতরাং, T dS = n Cv dT + P dV
 মূলত উপরের সমীকরণের উভয় পাশে নির্দিষ্ট যোগজীকরণ প্রয়োগ করে আমরা মোট এন্ট্রপির পরিবর্তনের মান বের করে ফেলতে পারি। প্রাথমিক অবস্থায় গ্যাসের চাপ, আয়তন, তাপমাত্রা ও এন্ট্রপির মান যথাক্রমে P1 , V1 , T1 ও S1 এবং সর্বশেষ অবস্থায় গ্যাসের চাপ, আয়তন, তাপমাত্রা ও এন্ট্রপির মান যথাক্রমে P2 , V2 , T2 ও S2 হলে (6) নং এর উভয়পাশে যোগজীকরণের সীমা হিসেবে এই মান গুলো বসালে –
মূলত উপরের সমীকরণের উভয় পাশে নির্দিষ্ট যোগজীকরণ প্রয়োগ করে আমরা মোট এন্ট্রপির পরিবর্তনের মান বের করে ফেলতে পারি। প্রাথমিক অবস্থায় গ্যাসের চাপ, আয়তন, তাপমাত্রা ও এন্ট্রপির মান যথাক্রমে P1 , V1 , T1 ও S1 এবং সর্বশেষ অবস্থায় গ্যাসের চাপ, আয়তন, তাপমাত্রা ও এন্ট্রপির মান যথাক্রমে P2 , V2 , T2 ও S2 হলে (6) নং এর উভয়পাশে যোগজীকরণের সীমা হিসেবে এই মান গুলো বসালে –
উপরে উল্লিখিত এই (7) নং সমীকরণই হল আদর্শ গ্যাসের বেলায় যেকোনো প্রক্রিয়ায় মোট এন্ট্রপির পরিবর্তন নির্ণয়ের সমীকরণ।
গ্যাসের ক্ষেত্রে আমরা মোটামুটি চার ধরণের প্রক্রিয়ার কথা আলোচনা করি-
১) সমোষ্ণ প্রক্রিয়া (Isothermal process) যেখানে তাপমাত্রা স্থির থাকে,
২) সমচাপীয় প্রক্রিয়া (Isobaric process) যেখানে চাপ স্থির থাকে,
৩) সমআয়তন প্রক্রিয়া (Isochoric process) যেখানে আয়তন স্থির থাকে,
৪) রুদ্ধতাপীয় প্রক্রিয়া (Isentropic process) যেখানে এন্ট্রপি স্থির থাকে ।
প্রতিটি প্রক্রিয়ার বেলাতেই আমাদের উপরে বের করা (7) নং সমীকরণ কাজ করে কিনা তা আমরা যাচাই করে দেখব। তার আগে এই সমীকরণের সুবিধা নিয়ে কিছু কথা বলে রাখি। এই সমীকরণ বের করার সময় আমরা গ্যাসের চাপ, আয়তন, তাপমাত্রা, এন্ট্রপি– এই চারটি রাশিকেই পরিবর্তনশীল ধরে নিয়েছিলাম।
১) সমোষ্ণ প্রক্রিয়ার বেলায় গ্যাসের অন্তর্নিহিত শক্তির মান পরিবর্তিত হয়না [ (4) নং থেকে ]। অর্থাৎ, dU=0
তাই, dQ=P dV বা, T dS=P dV
অতএব, আদর্শ গ্যাসের বেলায় যেকোনো প্রক্রিয়ায় এন্ট্রপি পরিবর্তনের সাধারণ সমীকরণ হিসেবে (7) নং সমীকরণকে আমরা নিশ্চিন্তে ব্যবহার করতে পারি।
 আদর্শ গ্যাসের বেলায় এন্ট্রপি পরিবর্তনের সাধারণ সমীকরণটি বুঝে গেলে আমরা খুব সহজেই এটি ব্যবহার করে বোল্টজম্যানের এন্ট্রপি-সূত্রে থাকা অজানা ধ্রুবকটি আদর্শ গ্যাসের জন্য কী হবে সেটা বের করে ফেলতে পারি।
আদর্শ গ্যাসের বেলায় এন্ট্রপি পরিবর্তনের সাধারণ সমীকরণটি বুঝে গেলে আমরা খুব সহজেই এটি ব্যবহার করে বোল্টজম্যানের এন্ট্রপি-সূত্রে থাকা অজানা ধ্রুবকটি আদর্শ গ্যাসের জন্য কী হবে সেটা বের করে ফেলতে পারি।
তার আগে কিছু নতুন জিনিস নিয়ে আলোচনা করি।
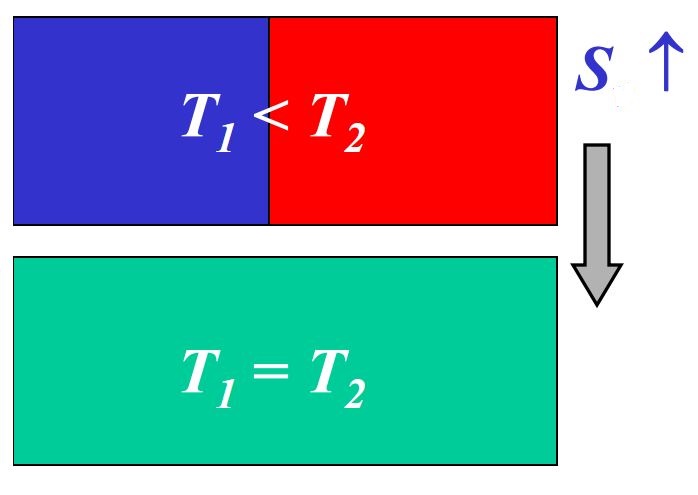
তাপগতিবিদ্যার দ্বিতীয় সূত্রকে কিছুটা ভিন্নভাবেও বর্ণনা করা যায়। তাপের সাথে জড়িত যেকোনো ঘটনা যে অবস্থাতেই থাকুক না কেন সেটা একটা নির্দিষ্ট অবস্থায় গিয়ে পৌঁছাতে চায়। এই নির্দিষ্ট অবস্থাকে সুন্দর ভাষায় বললে বলা হয় ‘সাম্যাবস্থা’(সাম্য অর্থাৎ সবাই সমান)। ব্যাপারটা বোঝা খুব সহজ। দু’টি বস্তুর তাপমাত্রা ভিন্ন ভিন্ন হলে তাদের যদি একে অন্যের সংস্পর্শে রাখা হয় তাহলে কিছু সময় পরে দেখা যায় তারা নতুন একটা নির্দিষ্ট তাপমাত্রায় গিয়ে পৌঁছে। গরম বস্তুটির তাপমাত্রা কমে, ঠাণ্ডা বস্তুটির তাপমাত্রা বাড়ে। দুইয়ে মিলে এমন একটা তাপমাত্রায় গিয়ে পৌঁছে যেটা তাদের উভয়ের প্রাথমিক তাপমাত্রার চাইতেই ভিন্ন- যেটা সময়ের সাথে সাথে আর পাল্টায় না। এই নতুন তাপমাত্রায় পৌঁছালে আমরা বলি যে বস্তু দু’টির তাপমাত্রা সাম্যাবস্থায় গিয়ে পৌঁছেছে। প্রথম বস্তুর তাপমাত্রাকে T1 ও দ্বিতীয় বস্তুর তাপমাত্রাকে T2 দিয়ে প্রকাশ করলে এবং প্রাথমিক অবস্থায়
T1 < T2 হলে, সাম্যাবস্থায় পৌঁছালে দেখা যাবে তাদের উভয়ের তাপমাত্রা সমান হয়ে গেছে। অর্থাৎ T1 = T2 হয়ে যাবে এবং সাথে সাথে মোট এন্ট্রপির পরিমাণও (S) বেড়ে যাবে।
বোল্টজম্যানের এন্ট্রপি সূত্র ব্যবহার করে সহজেই দেখানো যায় যে বস্তু দু’টি যখন সাম্যাবস্থায় পৌঁছায় তখন তাদের সেই অবস্থায় পৌঁছাতে পারার সম্ভাবনার মান সবচাইতে বেশি অর্থাৎ সম্ভাবনা এক (1) । ব্যাপারটা সহজে ব্যাখ্যা করি।
T1 তাপমাত্রায় থাকা কম তাপমাত্রার বস্তুটি যদি গরম বস্তুটি থেকে dQ পরিমাণ তাপ পেয়ে সাম্যাবস্থায় পৌঁছে এবং তার এন্ট্রপি dS1 পরিমাণ বাড়ে তাহলে
dS1 = dQ/T1
T2 তাপমাত্রায় থাকা গরম বস্তুটি থেকেই এই dQ পরিমাণ তাপ সরবরাহ হয়েছে বিধায় তার এন্ট্রপি যদি dS2 পরিমাণ কমে তাহলে
dS2 = -dQ/T2 (ঋণাত্মক চিহ্ন দিয়ে এন্ট্রপি কমেছে বোঝাচ্ছে)
এখন বোল্টজম্যানের এন্ট্রপি-সূত্র বলে
w এর সর্বোচ্চ মান হল এক বা 1 । তাই দেখা যাচ্ছে সাম্যাবস্থায় সম্ভাব্যতার মান সর্বোচ্চ অর্থাৎ 1। এখান থেকেই তাপগতিবিদ্যার দ্বিতীয় সূত্রের নতুন একটা বর্ণনা আমরা দিতে পারি আর সেটা হলো – “প্রতিটি প্রক্রিয়াই সাম্যাবস্থায় গিয়ে পৌঁছাতে চায় যেন তার সাথে জড়িত সম্ভাবনা এবং এন্ট্রপির মান সর্বোচ্চ হয়”।
এখানে উপরে দেখানো হিসাবের ব্যাপারে কিছু কথা বলে রাখি, না হলে মনের মাঝে কিছু কিছু অনাকাঙ্খিত প্রশ্নের জন্ম হতে পারে। লক্ষ্য করলেই দেখা যাবে যে সাম্যাবস্থায় সম্ভাব্যতার মান 1 বসালে এন্ট্রপির মান শূন্য হয়ে যাচ্ছে।
S = c ln(1) = 0
তাই কারো মনে প্রশ্ন আসাটা স্বাভাবিক যে এন্ট্রপির মান শূন্য হয় কীভাবে যেখানে তাপগতিবিদ্যার দ্বিতীয় সূত্র বলে যে এন্ট্রপির মান বাড়বে? এখানেই লুকিয়ে আছে ব্যাপারটার তাৎপর্য। c এর মান ধণাত্মক হলে S = c ln(w) সূত্রে সম্ভাব্যতা w এর মান এক অপেক্ষা কম বসালে ln(w) এর মান ঋণাত্মক হয়- ফলে এন্ট্রপির মান ঋণাত্মক হবে। সাম্যাবস্থায় সম্ভাব্যতা w যখন সর্বোচ্চ বা 1 তখন ln(w) এর মান শূন্য- ফলে এন্ট্রপির মানও শূন্য। এখন কেউ যদি পরিবর্তনের দিকে লক্ষ্য রাখে তাহলে দেখবে যে এন্ট্রপির মান ঋণাত্মক থেকে শূন্যের দিকে যাচ্ছে- অর্থাৎ বাড়ছে। যা আসলে তাপগতিবিদ্যার দ্বিতীয় সূত্রকে সমর্থনই করছে। তাই সাম্যাবস্থায় এন্ট্রপির মান শূন্য হয়ে গেছে দেখে ঘাবড়ানোর কিছু নেই। মোট এন্ট্রপির কিন্তু বৃদ্ধিই ঘটেছে শেষ পর্যন্ত।
এ কয়টি বিষয় মাথায় রেখে এখন আমরা আদর্শ গ্যাসের বেলায় বোল্টজম্যানের এন্ট্রপি-সূত্রে থাকা অজানা ধ্রুবকটির (c) মান বের করতে পারি।
ধরা যাক, এক মোল পরিমাণ আদর্শ গ্যাস V1 আয়তনের একটা পাত্রে রাখা আছে। V2 আয়তনের অন্য একটি খালি পাত্র এনে প্রথম পাত্রের সাথে সংযোগ ঘটাই যেন প্রথম পাত্রে থাকা গ্যাস দ্বিতীয় পাত্রের ভেতর সমানভাবে ছড়িয়ে পড়তে পারে। পুরো প্রক্রিয়াটি স্থির তাপমাত্রায় ঘটানোর ব্যবস্থা করি।
এখন, ঠিক যেই মুহূর্তে V1 আয়তনের পাত্রের সাথে V2 আয়তনের পাত্রটি যুক্ত করা হয়েছে ঠিক সেই মুহূর্ত থেকে আমরা এন্ট্রপির পরিবর্তন পরিমাপ করা শুরু করব যতক্ষণ পর্যন্ত না গ্যাসের অণুগুলো দুইটি পাত্রেই সমানভাবে ছড়িয়ে পড়ে। আরো সহজে বললে প্রাথমিক অবস্থায় গ্যাসের সবগুলো অণুই V1 আয়তনের মাঝে ছিল- যদিও মোট আয়তন তখন (V1 + V2) । সর্বশেষ অবস্থা ধরব তখনই যখন গ্যাসের সবগুলো অণুই পুরো (V1 + V2) আয়তন জুড়ে সমানভাবে ছড়িয়ে পড়ে।
এখন, আমরা প্রাথমিক অবস্থায় সবগুলো অণুকেই V1 আয়তনে খুঁজে পাওয়ার সম্ভাবনার মান (w1) বের করব।
————————————————————————————————————–
– লেখকঃ দীপায়ন তূর্য
(আরো সহজে বর্ণনা করার কোন উপায় জানা থাকলে নিঃসঙ্কোচে জানানোর অনুরোধ রইল।)
পরিশিষ্টঃ
আরো কিছু জানতে চাইলে –
১) http://www.eoht.info/page/S+%3D+k+ln+W
২) https://en.wikipedia.org/wiki/Boltzmann%27s_entropy_formula
৩) https://en.wikipedia.org/wiki/History_of_entropy
৪)http://web.mit.edu/16.unified/www/FALL/thermodynamics/notes/node56.html
৫) http://hyperphysics.phy-astr.gsu.edu/hbase/therm/entrop2.html
































অসংখ্য ধন্যবাদ! অনেক অনেক দোয়া রইল আপনাদের জন্য। জাযাকাল্লাহু খাইরান 🖤