এই লেখাটার মূল উদ্দেশ্য হলো, কীভাবে কোনো বস্তুর মাঝের বিশৃঙ্খলার পরিমাপ (এন্ট্রপি) বস্তুটির সেই অবস্থায় পৌঁছানোর সম্ভাবনার/সম্ভাব্যতার উপর নির্ভর করে সেটা বুঝা এবং তাদের মধ্যকার বিখ্যাত গাণিতিক সম্পর্ক, যেটা “বোল্টজম্যান-এন্ট্রপি সূত্র” নামে পরিচিত, সেটা সহজ ভাবে বুঝা এবং প্রমাণ করা।
মূল অংশে যাওয়ার আগে কিছু ছোট ছোট বিষয় আগেই বলে রাখি। তাপগতিবিদ্যার প্রথম সূত্র বলে যে, তাপশক্তি ব্যবহার করে কাজ করা যাবে এবং উল্টাভাবে কাজকেও তাপে পরিণত করা যাবে। এটা শক্তির নিত্যতা সূত্রেরই অন্য রূপ। কিন্তু এটা বলে না যে, তাপকে কতটুকু কাজে লাগানো যাবে। এখানেই তাপগতিবিদ্যার দ্বিতীয় সূত্রের আবির্ভাব।
দ্বিতীয় সূত্র বলে, তাপশক্তিকে কখনোই পুরোপুরি কাজে লাগানো যাবে না, যদিও কাজকে পুরোপুরি তাপে পরিণত করা যাবে। দ্বিতীয় সূত্র থেকেই আমাদের এই আলোচনার সূচনা।
মনে প্রশ্ন আসতে পারে এই যে, তাপকে যেহেতু পুরোপুরি কাজে লাগানো গেল না, তাহলে অকেজো অংশগুলো গেল কোথায়?
উত্তর হলো, এই অকেজো অংশগুলো শক্তির এমন কিছু রূপে পরিবর্তিত হয়, যেগুলোকে আর প্রয়োজনীয় কাজে রূপান্তর করা যায় না। শক্তির এই অংশটুকু হলো বিশৃঙ্খল অংশ, কারণ এই অংশটুকু নিয়ন্ত্রণ করা যায়না। নিয়ন্ত্রণ করা যায় না বলা হয় এ কারণে, যদি নিয়ন্ত্রণ করা যেত তাহলে তাকে কাজেও পরিণত করা যেত! যেহেতু তাকে আর কাজে লাগাতে পারছি না, তাই সেটা আর নিয়ন্ত্রণের মাঝেও নেই। এভাবেই বিশৃঙ্খলা ব্যাপারটা তাপের অকেজো অংশের সাথে আমরা যুক্ত করি।
এই বিশৃঙ্খলা বোঝার জন্য যে রাশিটা আমরা ব্যবহার করি, সেটা হলো এন্ট্রপি। এই রাশি কেন বিশৃঙ্খলার সাথে যুক্ত, সেটাও সহজে বুঝা উচিত। তাই এই রাশির ব্যাপারে আগে ছোট একটা আলোচনা করি।
এন্ট্রপির সবচেয়ে সহজ সংজ্ঞা ধাপে ধাপে এখান থেকে পাওয়া যায় – “বস্তুতে তাপ দিলে যদি তার তাপমাত্রা বাড়ে, তাহলে প্রতি একক তাপমাত্রায় যতটুকু তাপ বেড়েছে, সেটাই হলো এন্ট্রপির পরির্বতন”। দেখা যাচ্ছে, এন্ট্রপিকে একটা নতুন রকম রাশি চিন্তা করে তার পরিবর্তন কীভাবে মাপা যায়, তার ব্যাপারে বলা হয়েছে। মাথায় রাখতে হবে, এখানে কেবল এন্ট্রপির কতটুকু পরিবর্তন হয়েছে সেটা বলা হয়েছে। এন্ট্রপি আসলে নিজেই ব্যাপারটা কী, সেটা এখনো আসেনি। এই সংজ্ঞার পরের অংশেই ব্যাপারটা এসে পড়বে।
ধরলাম, ΔQ পরিমাণ তাপ দেওয়ার ফলে বস্তুর তাপমাত্রা T তে গিয়ে পৌঁছায়। তাহলে এন্ট্রপি বাড়লো S পরিমাণ। সাধারণত এন্ট্রপিকে ‘S’ দিয়ে প্রকাশ করা হয়। তাই এর পরিবর্তনকে লেখা হয় ΔS । সুতরাং,
এখন যদি কোন প্রক্রিয়ায় তাপের পরিবর্তন না হয়, তাহলে ΔQ= 0 , ফলে এন্ট্রপির পরিবর্তন ΔS=0 । এখন, যে প্রক্রিয়ায় তাপের পরিবর্তন হয় না, অর্থাৎ বাইরে থেকেও তাপ আসে না, আবার ভেতর থেকেও তাপ বের হতে পারে না, এমন প্রক্রিয়াকে বলা হয় রুদ্ধতাপীয় প্রক্রিয়া (রুদ্ধ মানে নিষেধাজ্ঞা, অর্থাৎ আটক অবস্থা। রুদ্ধতাপীয় মানে তাপের ভেতরে বা বাইরে যাওয়া নিষেধ)।
তাহলে দেখা যাচ্ছে, রুদ্ধতাপীয় প্রক্রিয়ায় এন্ট্রপির কোনো পরিবর্তন হয় না। অর্থাৎ আগে যা ছিলো, তাই থাকে। ঠিক এই জায়গা থেকেই এন্ট্রপির মূল সংজ্ঞাটা দেয়া যায়। যদি এন্ট্রপি একটা রাশি হয় (ভর, দৈর্ঘ্য, সময় – এগুলোর মত), তাহলে সেটার মান রুদ্ধতাপীয় প্রক্রিয়ায় পরিবর্তিত হয় না, বরং স্থির থাকে। তাই এন্ট্রপির সংজ্ঞায় উল্টাভাবে বলা হয়, “রুদ্ধতাপীয় প্রক্রিয়ায় কোনো বস্তুর মাঝে তাপের সাথে সম্পর্কিত যে রাশিটির মান স্থির থাকে, তাকেই এন্ট্রপি বলে”।
এখন আসি, কোনো তাপ প্রবাহের সাথে এন্ট্রপি বাড়ে নাকি কমে – সে প্রসঙ্গে। কারো মনে চিন্তা আসতে পারে, “যদি তাপ দেয়ার ফলে কোনো বস্তুর এন্ট্রপি বাড়ে, তাহলে কোনো বস্তু থেকে তাপ নিলে তো তার এন্ট্রপি কমার কথা!” হ্যাঁ, অবশ্যই কমে।
তাপ দিলে যদি ΔQ কে ধণাত্মক ধরা হয়, তাহলে তাপ বের হয়ে গেলে ΔQ কে ঋণাত্মক ধরতে হবে। তখন তার এন্ট্রপির পরিবর্তন ΔS-ও ঋণাত্মক হবে, অর্থাৎ এন্ট্রপি কমবে। এখন আসি আরো একটা ব্যাপারে। যে তাপটুকু বের হয়ে গেলো, সেটা নিশ্চয়ই অন্য কোনো বস্তু বা স্থানে গেছে! তাহলে সেই স্থানের এন্ট্রপি কিন্তু আবার বেড়ে গেলো। তাই আলাদাভাবে যদিও এন্ট্রপি বাড়তে বা কমতে পারে, কিন্তু যদি দুটো বস্তুর মোট এন্ট্রপির পরিবর্তন যোগ করে দেখা হয়, তাহলে দেখা যাবে মোট পরিবর্তনের মান ধনাত্মক হবে।
খুব সহজ একটা উদাহরণ দিয়ে এটা বুঝা যায়। তাপ সাধারণভাবে বেশি তাপমাত্রার জায়গা থেকে কম তাপমাত্রার জায়গায় প্রবাহিত হয়। ধরা যাক, T1 তাপমাত্রার গরম জায়গা থেকে ΔQ পরিমাণ তাপ T2 তাপমাত্রার অপেক্ষাকৃত ঠাণ্ডা জায়গায় গেছে। যেহেতু প্রথম গরম জায়গাটি কিছু তাপ হারিয়েছে, তাই তার এন্ট্রপি কমেছে। একে ΔS1 ধরা হলে,
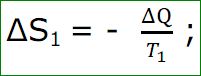
ঋণাত্মক চিহ্ন দেয়া হয়েছে তাপ কমার ব্যাপারটা বুঝানোর জন্য। এখন এই তাপ যেহেতু দ্বিতীয় বস্তু পেয়েছে, তাই তার এন্ট্রপি বেড়েছে। একে ΔS2 ধরা হলে,

সুতরাং পুরো প্রক্রিয়ায় মোট এন্ট্রপির পরিবর্তন = ΔS1 + ΔS2
অর্থাৎ পুরো প্রক্রিয়ায় মোট এন্ট্রপির পরিবর্তনও ধনাত্মক। এখান থেকেই সাধারণ সিদ্ধান্তে আসা যায় যে, তাপের প্রবাহ সম্পর্কিত যেকোনো ঘটনা ঘটলে সেই প্রবাহের সাথে সম্পর্কিত সবগুলো বস্তুর এন্ট্রপির পরিবর্তন যোগ করলে তার মান ধনাত্মক হবে। আর যদি তাপের প্রবাহ না থাকে (যেমন রূদ্ধতাপীয় প্রক্রিয়ায়) তাহলে তার পরিবর্তন হবে শূন্য। গাণিতিকভাবে বললে,
যেকোনো প্রক্রিয়ায় ΔS ≥ 0
যেহেতু দেখা যাচ্ছে, কিছু একটা ঘটলেই তার সাথে যুক্ত থাকা মোট এন্ট্রপির পরিবর্তনের মান কোনোমতেই কমানো যাবে না, তাই ব্যাপারটা নিয়ন্ত্রণের কোন সুযোগ নেই। অর্থাৎ ব্যাপারটা আমাদের হাতের বাইরে, বা শৃঙ্খলিত না। সেজন্যই একে বিশৃঙ্খলার পরিমাপক হিসেবে ধরা হয়।
এখন এন্ট্রপির ব্যাপারটা আলোচনা করতে গিয়ে যেহেতু নিয়ন্ত্রণ কিংবা নিয়ন্ত্রণহীনতার কথা উঠে এসেছে, তাই এই কথার সূত্র ধরেই আমরা এর সাথে সম্ভাবনা বা সম্ভাব্যতার ব্যাপারটা আনতে পারি। উদাহরণ হিসেবে সম্ভাব্যতার একটা ছোট উদাহরণ দেয়া যায়।
যদি ৫টা সবুজ কলম থেকে কাউকে যেকোনো একটা বেছে নিতে বলা হয়, তাহলে তার একটা সবুজ কলম পাবার সম্ভাবনাই একদম পুরোপুরি থাকে। কিন্তু যদি ৩টা সবুজ ও ২টা বেগুনী কলম থেকে যেকোনো একটা বেছে নিতে বলা হয়, তাহলে বেছে নেয়া কলমটি সবুজ হবার সম্ভাবনা কমে যায়। প্রথম ক্ষেত্রে সবুজ কলম পাবার পুরো ব্যাপারটার উপর পূর্ণ নিয়ন্ত্রণ ছিল, কিন্তু দ্বিতীয় ক্ষেত্রে সবুজ কলম পাবার উপর নিয়ন্ত্রণটুকু কমে গেছে। তাহলে দেখা যাচ্ছে, সম্ভাবনার সাথে গাণিতিকভাবে নিয়ন্ত্রণের ব্যাপারটা যুক্ত। আবার একটু আগেই আমরা এন্ট্রপির সাথেও যে নিয়ন্ত্রণের ব্যাপারটা (শৃঙ্খলা বা বিশৃঙ্খলা) জড়িত, সেটা বলেছি। তাহলে একটু ভাবলেই এই ধারণাটা বুঝা যায় যে, এন্ট্রপির সাথেও কোনোভাবে হয়ত সম্ভাব্যতার বিষয়টা জড়িত থাকতে পারে।
আরো সহজভাবে বললে বলা যায়, একই তাপমাত্রায় রাখা পাশাপাশি দুটো বস্তুর মাঝে যেটাতে এন্ট্রপির বৃদ্ধি বেশি হয়েছে, সেখানে বিশৃঙ্খলা বেশি বলে সেখান থেকে তাপের রূপান্তরের মাধ্যমে দরকারি কাজ পাওয়ার সম্ভাবনা অন্য বস্তুটির তুলনায় কমে যাবে। যদি ধরে নিই এন্ট্রপির মান বস্তুটির সেই অবস্থায় পৌঁছানোর সম্ভাব্যতার উপর নির্ভরশীল, তাহলে গাণিতিকভাবে এন্ট্রপিকে সম্ভাব্যতার যেকোনো একটি ফাংশন ধরা যায়। ‘যেকোনো’ বলার কারণ হলো, আমরা এখনো নির্দিষ্টভাবে সেই ফাংশনটি কেমন, তা জানি না। তাই সম্ভাব্যতাকে ‘ω’ দিয়ে প্রকাশ করে এন্ট্রপিকে (S) যদি সম্ভাব্যতার যেকোনো ফাংশন f ধরা হয় তাহলে,
S = f(ω)
এখন ধরি, একটি বস্তুর এন্ট্রপির মান S1 এবং তার সম্ভাবনার মান ω1 এবং অন্য একটি বস্তুর এন্ট্রপির মান S2 এবং তার সম্ভাবনার মান ω2 ; তাহলে তাদের মাঝে ফাংশন f দিয়ে সম্পর্ক স্থাপন করলে,
S1 = f(ω1) এবং S2 = f(ω2)
এই অংশে এসে আমরা সম্ভাব্যতার একটি সাধারণ বৈশিষ্ট্য ঝালাই করে নেবো। দুটি ঘটনা একসাথে ঘটার সম্ভাবনা তাদের আলাদা আলাদাভাবে ঘটার সম্ভাবনার গুণফলের সমান। ব্যাপারটা সহজ করে বুঝার জন্য উদাহরণ হিসেবে একটা ভিন্ন বিষয় দিয়ে শুরু করা যাক।
ধরা যাক A, B এবং C তিনটা ভিন্ন ভিন্ন স্থান। A থেকে B তে যাওয়ার ৩টি পথ আছে। তাদের নাম p, q, এবং r । B থেকে C তে যাওয়ার ২টি পথ আছে। তাদের নাম m এবং n । কোন ব্যক্তি যদি A থেকে B তে গিয়ে তারপর C তে পৌঁছাতে চায়, তাহলে সে মোট ৩x২=৬ উপায়ে সেটা করতে পারে (pm, pn, qm, qn, rm, rn)। দেখা যাচ্ছে, একস্থান থেকে অন্যস্থানে যাওয়ার পথের সংখ্যাগুলোকে গুণ করে দিলেই মোট কতভাবে যাওয়া যায়, সেটা বের হয়ে যায়।
একই কথা পরপর দু’টা ঘটনা ঘটার সম্ভাবনার বেলাতেও প্রযোজ্য। যেমন, একটা সবুজ ও দু’টি খয়েরী রঙের মোট তিনটা বল থেকে খয়েরী রঙের বল আসার সম্ভাবনা 2/3 (2=খয়েরী বলের সংখ্যা, 3=মোট বলের সংখ্যা)। একই ভাবে একটা নীল বল ও একটা বেগুনী বল থেকে বেগুনী বল আসার সম্ভাবনা ½ । এখন, প্রথমবার ঠিক খয়েরী এবং এর পরের বার ঠিক বেগুনী আসার সম্ভাবনা হবে 2/3 x 1/2 = 2/6 = 1/3 । এটাকে সহজে এভাবেও ব্যাখ্যা করা যায়, প্রথম তিনটা বল ও পরের দু’টা বলকে মোট ৩x২=৬ উপায়ে নেয়া যায় [(সবুজ ,নীল), (সবুজ ,বেগুনী), (খয়েরী ১ম, নীল), (খয়েরী ১ম, বেগুনী), (খয়েরী ২য়, নীল), (খয়েরী ২য়, বেগুনী)]। এই ৬টা উপায়ের মাঝে আমাদের দরকার প্রথমে খয়েরী ও পরে লাল। এদের পাওয়া যেতে পারে ২x১=২ ভাবে [(খয়েরী ১ম, বেগুনী), (খয়েরী ২য়, বেগুনী)]। তাই প্রথমবার ঠিক খয়েরী এবং এর পরের বার ঠিক বেগুনী আসার সম্ভাবনা হবে 2/6 = 1/3, যা আসলে দু’টা সম্ভাবনার গুণফল।
এখন যদি S1 এন্ট্রপির বস্তুর সাথে S2 এন্ট্রপির বস্তুকে রাখা হয়, তবে তাদের মোট এন্ট্রপি হবে S = S1+S2। শেষ অবস্থায় পৌঁছানোর সম্ভাব্যতা যদি ‘ω’ হয়, তাহলে সম্ভাব্যতার নিয়মে তা হবে দুটি বস্তুর আলাদাভাবে সম্ভাব্যতার গুণফলের সমান। অর্থাৎ ω= ω1 x ω2 । f এর ফাংশন আকারে S = S1+S2 কে লিখলে দাঁড়াবে
f(ω)= f(ω1) + f(ω2)
বা, f(ω1 x ω2)= f(ω1) + f(ω2)
উপরের সমীকরণে দেখা যাচ্ছে, এটি দুটি পারস্পরিক সম্পর্কবিহীন চলক ω1 ও ω2 -এর সমন্বয়ে তৈরি। এখানে আমরা ক্যালকুলাসের দুটি সহজ বিষয় প্রয়োগ করবো। প্রথমটা হলো, ‘অব্যক্ত ফাংশনের অন্তরীকরণ (Implicit function)’ এবং পরেরটা হল ‘ফাংশনের ফাংশান এর অন্তরীকরণ (function of a function)’ [এগুলোর ধারণা পোক্ত হলে সামনের অংশে আগানো যাবে। এগুলোর ব্যাখ্যা সহজ করার জন্য লেখার শেষে কিছু ওয়েব লিংক দিয়ে দেয়া আছে]।
যেহেতু সমীকরণ থেকে কেউ চট করে ω1 এবং ω2 এর মাঝে একটাকে দিয়ে অন্যটাকে সরাসরি প্রকাশ করতে পারবেনা [যেমন ω1 = g(ω2) বা ω2 = h(ω1) আকারে, যেখানে g এবং h অন্য দুটি ফাংশন] তাই f(ω1 x ω2)= f(ω1) + f(ω2) এর উভয় পাশকে প্রথমে ω1 এর সাপেক্ষে অন্তরীকরণ করলে পাওয়া যাবে
ω2 x f’(ω1 x ω2)= f’(ω1) + 0 [ f’ দিয়ে প্রথম অন্তরক সহগ বুঝানো হচ্ছে ]
বা, ω2 x f’(ω1 x ω2)= f’(ω1) ———-(1)
একই ভাবে f(ω1 x ω2)= f(ω1) + f(ω2) এর উভয়পাশকে ω2 এর সাপেক্ষে অন্তরীকরণ করলে পাওয়া যাবে
ω1 x f’(ω1 x ω2)= f’(ω2) ———– (2)
(1) কে (2) দিয়ে ভাগ করলে
বা, ω1 x f’(ω1) = ω2 x f’(ω2)
উপরের সম্পর্ক একটু ভালভাবে পর্যবেক্ষণ করলে বুঝা যাবে প্রথম বস্তুর সম্ভাব্যতা ও এন্ট্রপি ফাংশনের প্রথম অন্তরকের গুণফল এবং দ্বিতীয় বস্তুর সম্ভাব্যতা ও এন্ট্রপি ফাংশনের প্রথম অন্তরকের গুণফল একই। সাধারণভাবে বললে যেকোন বস্তুর সম্ভাব্যতা ও এন্ট্রপি ফাংশনের প্রথম অন্তরকের গুণফল সবসময় একই থাকছে। অতএব, এই গুণফলকে যে কোনো ধ্রুবক C ধরে নিলে এবং শেষ অবস্থার উপর সেটা প্রয়োগ করলে,
এবার উভয়পক্ষে ω এর সাপেক্ষে যোগজীকরণ করলে পাওয়া যাবে,


এখন মান বের করার জন্য আমরা এন্ট্রপি এবং সম্ভাব্যতার মূল ধারণাটা প্রয়োগ করবো।
যদি কোন বস্তুর ভেতরকার শক্তির অবস্থার ব্যাপারে আমরা সম্পূর্ণ নিশ্চিতভাবে জানি, তাহলে তার সম্ভাব্যতা হবে 1 । যেহেতু বস্তুটির ব্যাপারে আমরা পুরোপুরি নিশ্চিত, তাই বস্তুটি পুরোপুরি একটি সুশৃঙ্খল বস্তু। তার মাঝে কোন বিশৃঙ্খলা নেই। আর বিশৃঙ্খলা না থাকায় তার মাঝে কোন এন্ট্রপিও থাকবে না, অর্থাৎ এন্ট্রপির মান হবে শূন্য (0)।
সুতরাং ω =1 হলে S = 0 । এইদুটি মান (3) নং সমীকরণে বসালে,
0= C ln(1)+CM বা, 0= 0 + CM বা, CM=0
CM এর মান (3) নং সমীকরণে বসালে অবশেষে আমাদের কাঙ্ক্ষিত এন্ট্রপি এবং সম্ভাব্যতার মধ্যকার সম্পর্ক পাওয়া যাবে। সেটি হলো,
এটিই হল বোল্টজম্যানের বিখ্যাত এন্ট্রপি-সূত্র।
এই সূত্র প্রয়োগের আগে কিছু পর্যালোচনা করা দরকার, না হলে ভুলভাবে ব্যবহারের সম্ভাবনা থেকে যায়। যেমনঃ
১) যে কোনো জিনিস ঘটার সম্ভাবনার মান (ω) 1 এর চেয়ে কম বা 1 এর সমান। তাই ω এর মান 1 এর চেয়ে কম হলে ln (ω) এর মান ঋণাত্মক। কিন্তু এন্ট্রপির মান কোনোভাবেই ঋণাত্মক হতে পারবে না। এই সমস্যা দূর করা হয় ধ্রুবক C এর মাধ্যমে। C এর মান যেহেতু আমরা জানি না, তাই সেটার মান ধনাত্মক বা ঋণাত্মক যে কোনোকিছুই হতে পারে। তাই যুক্তি থেকে বলা হয়, ln (ω) এর সহগের মান ঋণাত্মক হবে। তাই মূল সূত্রটি লেখার সময় একটা ঋণাত্মক চিহ্ন এনে দেখানো হয়। কেবল তখনই C এর মান ধনাত্মক হবে।
সুতরাং, S = C ln ( ω ) ; C ঋণাত্মক
অথবা, S = – C ln (ω ); C ধণাত্মক
২) কেবলমাত্র আদর্শ গ্যাসের ক্ষেত্রে C এর মান অণুপ্রতি গ্যাস ধ্রুবক বা বোল্টজম্যান-ধ্রুবক k এর সমান হয়। (k= R/NA ; R = আদর্শ গ্যাস ধ্রুবক, NA = এভোগ্যাড্রো সংখ্যা)। এর ব্যাখ্যা পরের নোটে বলার আশা রাখি।
—————————————————
আরো সহজে বর্ণনা করার কোনো উপায় জানা থাকলে নিঃসঙ্কোচে জানানোর অনুরোধ রইলো —- দীপায়ন তূর্য
























মাথা পুরাই আওয়ালা হয়ে গেছে
🙂 🙂 🙂 🙂 🙂 🙂 🙂
আচ্ছা, তাহলে w হল সিস্টেম থেকে কাজ পাওয়ার সম্ভাব্যতা আবার এটি সিস্টেমের শৃঙ্খলার মাত্রা।
এখন, এই w বিষয়টা নিয়ে বিস্তারিত লখখলে, অর্থাৎ বিভিন্ন উদাহরণের মাধ্যমে বিষয়টা দেখালে খুশি হতাম।
আদর্শ গ্যাসের বেলায় C এর মান নির্ণয় এর উপর একটা নোট ছিল। ওটা একটা উদাহরণ। 🙂
[…] বিশৃঙ্খল হয়ে যাওয়া অংশ। একেই বলে এন্ট্রপি। গাণিতিক প্রমাণ অনুসারে এন্ট্রপি […]
চমৎকার লিখেছেন। আরো লিখবেন এই প্রত্যাশায়-
আচ্ছা। ^_^
এখানে পরের কয়েকটা লেখা আছে।
https://bigganjatra.org/writer/turja/
এগুলোর বাইরে নীচের ওয়েবসাইটে দিচ্ছি।
https://deepayanturja.wordpress.com/
porer note er link den.
এখানে আছে। 🙂
https://bigganjatra.org/writer/turja/
এগুলোর বাইরে নীচের ওয়েবসাইটে দিচ্ছি।
https://deepayanturja.wordpress.com/
eta kivabe bekkha korse vai?
Nice..